A Anvisa (Agência Nacional de Vigilância Sanitária) proibiu, nesta segunda-feira (4), a comercialização do hidratante facial “Skin face – Clareador Noite“, fabricado por uma empresa não identificada.
Também foi definida a apreensão de todos os lotes do produto e as medidas contra o creme já estão em vigor. No diário oficial, a Agência explicou que a empresa fabricadora não tem registro ou autorização para produção do hidratante – infringindo leis do país – além de o próprio produto não ter registro sanitário.
Foram proibidos a comercialização, a distribuição, a fabricação, a propaganda e o uso do creme.
Recomendamos para você

Empresa de engenharia abre vagas em Goiás
Vagas são para profissionais de nível técnico e superior, com oportunidades abertas em Go...
Publicado em 2026-05-05 20:05:35
Justiça do Reino Unido condena ativistas pró-Palestina por ataque violento a empresa israelense
Justiça britânica condena ativistas por ataque criminoso a empresa israelense que causou danos mil...
Publicado em 2026-05-05 19:50:57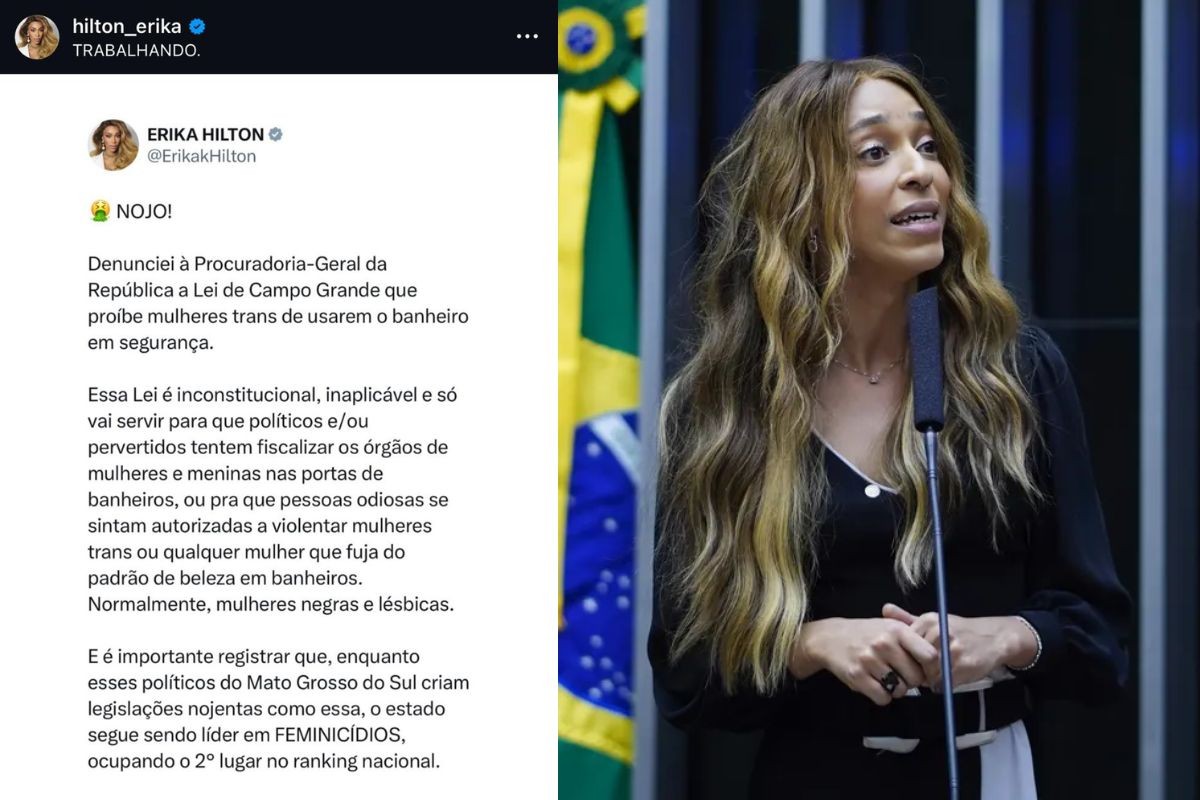
Erika Hilton denuncia à PGR lei que proíbe mulheres trans usarem banheiros femininos em Campo Grande
Deputada publicou nas redes sociais que fez denúncia à PGR Redes sociais/Pablo Valadares/C...
Publicado em 2026-05-05 19:34:40Caneta emagrecedora de alta dose recebe aprovação da Anvisa no Brasil
Anvisa atualiza regras de pesquisas clínicas; entenda as mudanças
A Anvisa aprovou uma atualização sobre as regras que regulam a pesquisa clínica no Brasil. As novas normas devem permitir uma maior atratividade do Brasil para investimentos nesse tipo de pesquisa.
Segundo a agência reguladora, a pesquisa clínica engloba o conjunto de estudos feitos com seres humanos, sendo que os dados gerados durante esses estudos servem para demonstrar a eficácia e a segurança de um medicamento que, durante a fase da pesquisa, é considerado um produto sob investigação.
“Os estudos clínicos são um dos pilares centrais para o registro de novos medicamentos e sua chegada ao mercado”, afirmou a agência. A proposta foi aprovada pela diretoria colegiada da Anvisa no último dia 27 de abril.
A atualização das regras foi proposta pela própria área técnica da agência e contou com 240 contribuições durante a fase de consulta pública, sendo todas analisadas individualmente pela equipe técnica.


